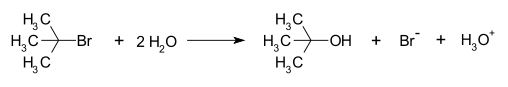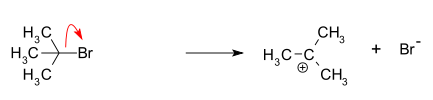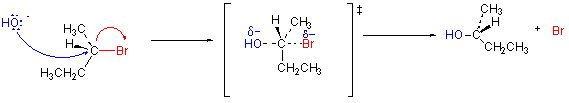SN1, SN2 반응에 대해 설명해보세요.
SN1, SN2 반응은 둘 다 치환반응이지만 반응 메커니즘 상 전혀 다른 과정을 거쳐서 진행되므로 여러 가지 다른 특성을 보인다.
SN1 반응은 반응 중에 중간체로 불안정한 탄소 양이온이 생성된 후 염기나 용매와 반응하여 치환체가 생성되는데, 첫 번째 단계가 속도 결정단계이므로, 반응속도식에서 기질의 농도만이 반응속도에 관여하므로 1차 반응이고, SN2 반응은 반응이 중간체를 형성하지 않고 친핵체가 바로 기질을 공격하여 이탈기가 떨어져나가며 치환 반응이 일어나는 경우이다. 이때는 기질과 친핵체의 농도가 모두 반응속도에 영향을 미치므로 2차 반응이다.
메커니즘 상에서 SN1 반응의 경우는 탄소 양이온 생성단계가 반응의 반응속도 결정단계이므로 탄소 양이온의 안정성이 바로 반응성과 일치한다. 즉 3차, 2차, 1차 순으로 반응성이 나타난다. 실제 특수한 경우를 제외하고 1차인 경우 Sn1 반응이 거의 진행하지 않는다. Sn2 반응에서는 기질이 얼마나 Nu에 공격당하기 쉬운가가 반응속도의 척도가 되므로 상대적으로 탄소를 공격하기 쉬운 구조인 1차, 2차, 3차 순서로 반응이 잘 일어난다.
SN1 반응에서 C-X의 C가 chiral carbon(부제성탄소)라면 carbocation 형성으로 반응이 진행되므로 base가 평면 carbocation의 양쪽에 다 붙을 수 있으므로 결국 라세미 화합물을 생성하게 된다. SN2 반응은 반응의 전이 상태에서 Nu의 backside attack(후면공격, 전자끼리의 반발)에 의한 inversion(반전)이 일어나므로 생성물은 configuration이 바뀌게 된다.
용매는 기질이나, 염기, 반응 중간체와 항상 interaction을 하고 있기 때문에 반응에 영향을 미치게 되는데, SN1 반응에서 반응의 속도 결정단계인 carbocation 생성단계에서 탄소 양이온을 안정화시킬 수 있는 용매가 반응에 더 유리하다. 즉 쌍극자 δ- δ+를 가지는 극성 양자성 용매(H2O, CH3OH 등)가 carbocation과 떨어져나간 L group을 안정화 시킬 수 있으므로, 더 유리하다.
SN2 반응에서는 Nu가 기질을 back-side attack 하는 단계에서 만일 물과 같은 δ+를 가지는 경우, Nu를 둘러싸서 오히려 Nu의 기질 공격을 방해하기 때문에, 쌍극자를 가지지 않는 DMF(dimethylformaide), THF(tetrahydorfurane)같은 용매가 유리하다.
유기화학 반응은 SN1, SN2, E1, E2 네 가지의 반응으로 분류된다.
(1) SN1 반응
SN1 반응은 유기화학에서의 치환반응의 한 종류이다. SN1 반응에서 SN은 친핵성 기질을 의미하고 1은 속도결정단계에 한 종류의 분자가 관여하기 때문에 붙여진 이름이다. SN1 반응은 반응 중간체로 탄소 양이온이 존재하는 경우가 많고 2차 또는 3차 할로알케인의 반응에서 자주 볼 수 있다. 강한 산성 환경에서는 2차 또는 3차 알코올도 SN1 반응을 일으킬 수 있다. 1차 할로알케인의 경우에는 SN2 반응이 일어난다. 일반적으로 SN1 반응에서는 기질이 해리되어 탄소 양이온을 만드는데, 이 단계가 속도결정단계가 된다. 이후 친핵체가 탄소 양이온을 공격하여 치환반응이 완결된다. 탄소 양이온이 삼각 평면 구조를 가지기 때문에 결과물은 R형, S형이 모두 나타나는 라세미체가 생성되어야 하지만 이온쌍의 관여에 의해 완전한 라세미화가 이루어지는 경우는 많지 않다.
SN1 반응의 메커니즘(mechanism)의 한 예시로 tert-butyl bromide와 물은 SN1을 통해 tert-butyl alcohol이 된다.
tert-butyl bromide는 C-Br 결합이 불균형적으로 분해되면 중간체인 탄소 양이온이 만들어진다. 이 단계가 가장 느려서 전체 반응 속도를 결정한다. 이 과정에서 나온 브로민 음이온은 이탈기(a leaving group)이 된다.
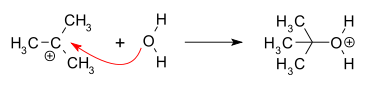
친핵체 공격: 탄소 양이온에 전자가 상대적으로 풍부한 산소가 친핵체가 되어 양전하를 띄는 중심탄소를 공격하여 결합이 형성된다.
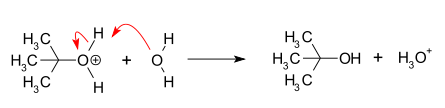
O-H결합에 관여하는 전자가 산소 쪽으로 옮겨가고 수소양이온은 떨어져 나와 물과 만난다. 이로써 반응이 종결된다.
(2) SN2 반응
SN2 반응의 메커니즘은 한 단계 반응으로서 친핵체 (식 1에서는 :OH-)가 이탈기의 반대 방향에서 접근하여 일어나는데, 친핵체의 접근과 이탈기의 이탈 반응이 한 단계, 즉 동시에 일어난다는 것이다.
(3) E1 반응
E1 반응은 two-step process로 일어난다. SN1 반응과 마찬가지로 천천히 일어나며 (rate-limiting step), 이탈기(leaving group)이 제거되면서 탄소 양이온(carbocation)을 형성한다. 그 다음 반응은 두 반응 즉, SN1과 E1 반응이 가능하다.
(4) E2 반응
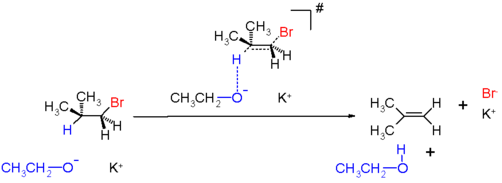
E2 반응은 유기화학에서의 제거 반응의 메커니즘 중 하나이다. E2 반응이 일어나게 되면 알켄이나 알카인이 생성된다. 염기의 공격에 의해 알케인이나 알켄의 수소 하나가 떨어져 나간다. 이와 동시에 수소와 공유결합을 하고 있던 전자는 탄소-탄소 파이 결합을 형성하게 된다. 이와 동시에 수소를 달고 있던 탄소 바로 옆의 이탈기를 달고 있던 탄소에서 이탈기가 탄소와 공유하던 전자쌍을 가지고 떨어진다. 결론적으로 염기에 의해 수소가 떨어지는 동시에 여기서 나온 전자쌍에 의해 파이 결합 형성과 동시에 이탈기가 떨어져 나가는 것이다.
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기