수득률에 대해 말해 보십시오.
반응 물질이 완전히 반응하였을 때 기대되는 생성 물질의 양을 100으로 보았을 때 실제 생성된 물질의 양을 그 반응의 수득률이라고 한다. 대부분의 화학 반응은 가역적으로 진행하기 때문에 반응 물질과 생성 물질이 공존하는 화학 평형에 도달한다. 따라서 수득률은 100%가 될 수 없다. 그러나 화학 물질을 생산하는 화학 공장에서는 원료의 효율을 극대화하기 위하여 수득률을 높이는 조건을 찾아야 한다. 수득률은 평형 이동에 의하여 높일 수 있다.
[수득률이 100이 될 수 없는 이유]
(1) 제품이 모두 결정화 되어 석출되지 않고 모액(Mother Liquid)에 용해된 상태로 제품이 있기 때문이다. (용해도가 0이 아니며, 특히 순도가 떨어지면 이물질과 함께 모액에 용해된 상태로 남아 있는 양이 늘어남)
(2) 여과 후 결정을 세척할 때 세척용액에 용해되어 손실되는 양이 있기 때문이다. (Rinsing 과정에서 나온 용액은 농축한 후 재결정하여 회수 필요함)
(3) 실험기구나 장치 등에 묻어 손실되는 양이 있기 때문이다. (이 양은 실험규모가 늘어나면 상대적으로 크게 줄어들 수 있음)
[암모니아와 수득률]
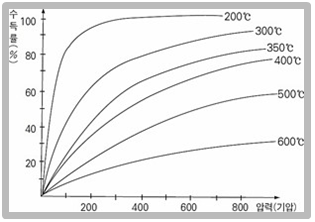
암모니아가 생성되는 반응에서 수득률을 높이려면 평형이 정방향(오른쪽)으로 이동할 수 있는 조건을 만들어야 한다.
이 반응에서 정반응이 일어날 때 분자 수가 감소하고 열이 방출되므로 암모니아의 수득률을 높이기 위해서는 압력을 높이고 온도를 낮추어야 한다. 일반적으로 수득률을 높이기 위해서는 다음과 같이 화학 반응식의 계수와 반응열을 고려한다.
aA(g)+bB(g) ⇄ cC(g)+dD(g)에서 분자 수가 증가하는 반응(a+b<c+d)이면 압력을 낮추고, 분자 수가 감소하는 반응(a+b>c+d)이면 압력을 높인다. 또한 발열 반응(Q>0)이면 온도를 낮추고, 흡열 반응(Q<0)이면 온도를 높인다. 화학 반응을 산업에 이용할 때에는 수득률과 반응 속도를 동시에 고려하여야 한다.
암모니아 생성 반응에서 수득률을 높이기 위해서는 온도를 낮추어야 하지만 온도가 낮으면 반응이 느리게 진행하므로 비효율적이다. 그렇다고 온도를 높이면 반응은 빠르게 진행되지만 수득률이 지나치게 낮으므로 곤란하다. 실제로 암모니아 합성 공장에서는 반응 속도가 지나치게 느려지지 않을 정도로 온도를 유지하여 반응시키며, 이 대신 반응 속도가 느려지는 것을 방지하기 위하여 촉매를 사용하고 있다.
[수득률 예제]
<문제>
2.00g의 살리실산을 4.00g의 무수아세트산과 가열하면 아스피린의 이론적 수득량은 얼마인가?
실험식에서 산리신산과 무수아세트산이 1:1로 반응하기 때문에 반응물들의 몰량을 계산하여
생성물의 몰량을 알 수 있다.
산리실산 분자량 = 138.07g/mol(C7=84.07 H6=6 O3=48)
산리실산 몰량= 2g / 138.07g/mol=0.014mol
무수아세트산 분자량=102.4g/mol(C4=48.04 H6=6 O3=48)
무수아세트산 몰량= 4g / 102.4g/mol=0.039mol
산리실산 0.014mol과 무수아세트산 0.014mol이 반응해서 아스피린 0.014mol과 초산 0.014mol이 생성된다. 여기서 아스피린 생성된 몰수에다 분자량을 곱해주면 생성되는 아스피린의 량을 구할 수 있다
0.014mol * 180.09 g/mol
= 2.52g
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기