할로겐원소의 특징에 대해 설명해보세요.
할로겐 원소는 원자번호가 작을수록 원자 반지름이 작기 때문에 전자와의 거리가 짧아서 상호 인력이 커져 음이온이 되려는 성질이 크다. 할로겐 원소의 일반적인 성질은 다음과 같다.
이온화 에너지 크기: F > Cl > Br > I
전자 친화도의 크기: Cl > F > Br > I
반응성의 크기: F2 > Cl2 > Br2 > I2
결합 에너지 크기: HF > HCl > HBr > HI
물에 대한 용해도: F2 > Cl2 > Br2 > I2
해설 및 핵심용어정리
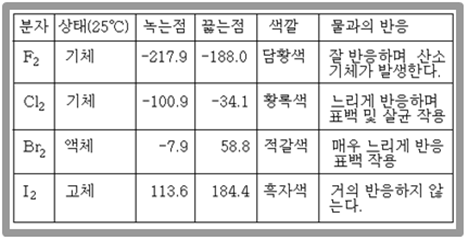
할로겐 원소는 주기율표에서 17족의 원소로 F, Cl, Br, I로 이루어져 있다. 할로겐 원소는 각각 고유의 색깔을 나타내며 유독하다(플루오르-담황색, 염소-황록색, 브롬-적갈색, 요오드-흑자색). 상온에서는 : F2 , Cl2 , Br2 , I2와 같이 2원자 분자의 형태로 존재한다. 전자 1개를 얻어 (-1)의 음이온이 되기 쉽다. 반응성이 커서 알칼리 금속이나 수소와 직접 반응한다. 할로겐 원소의 수소화물은 물에 녹아 산성을 나타낸다. 할로겐 원소의 일반적인 성질은 다음 표와 같다.
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기