고분자 화합물 합성 과정에 대해서 말해 보십시오.
저분자 화합물끼리 반응하여 단위 구조가 반복되는 고분자 화합물이 되는 반응을 중합(polymerization)이라고 한다. 이를 반응 형태에 다라 축합 반응, 부가 반응, 개환중합반응으로 구분된다. 먼저 축합 반응은 둘 이상의 분자들이 서로 반응하여 물이나 암모니아 등을 동시에 잃으면서 반응하는 것을 말한다. 주로 나일론(nylon), 폴리에스테르, 페놀수지, 요소수지 등이 축합 반응으로 고분자가 된다. 그리고 부가반응은 올레핀이나 카르보닐 화합물들이 반응하여 고분자가 되는 반응이다. 그리고 개환중합반응은 고리가 열리거나 또는 고리가 열린 뒤 자라나는 사슬 끝에 선형 생성물을 부가하는 방식으로 일어난다. 사슬이 성장하는 반응인 부가 반응은 성장 말단의 종류에 따라 라디칼 중합 반응, 양이온 중합 반응, 음이온 중합 반응 등이 가능하며 축합 반응에는 중축합, 중부가, 부가축합 반응 등이 가능하다. 개환중합반응도 다양한 반응이 가능하며 이 외에도 복분해, 고분자 치환 등 매우 다양한 방법으로 고분자를 중합할 수 있다.
해설 및 핵심용어 정리
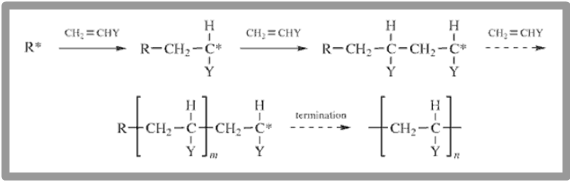
고분자는 제조 방법에 따라 첨가 고분자(addition polymer)와 축합 고분자(condensation polymer)로 구분할 수 있다. 보통 첨가 고분자를 사슬 반응(chain reaction)에 따른 연쇄 중합(chain polymerization)으로 만들 수 있어서 사슬 성장 고분자(chain-growth polymer)라고도 부르고 축합 고분자는 축합 반응(condensation reaction)으로 만들 수 있어서 단계 성장 고분자(step-growth polymer)라고 부르지만 반드시 그러한 것은 아니니 주의해야 한다. 그러나 일부 예외적인 경우를 제외하면 거의 동의어로 사용된다. 연쇄 중합(chain polymerization)은 단량체가 붙는 것이 마치 사슬과 같다고 하여 지어진 이름이다. 성장하는 고분자 사슬의 끝에 단량체가 계속 첨가되기 때문에 이러한 이름이 붙었다. 이러한 사슬의 끝은 라디칼(radical)일수도 있고 양이온이나 음이온일 수도 있기 때문에 반응성이 있다. 예를 들어 라디칼 R*에서부터 시작되는 사슬 반응은 다음과 같다.
위의 첨가 반응에서 Y는 각 단량체마다 다르다. 대표적인 사슬반응의 단량체와 반복구조(repeating unit), 고분자 이름은 다음과 같다.
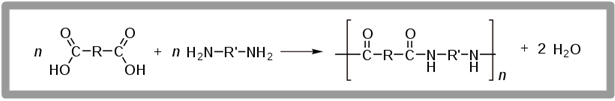
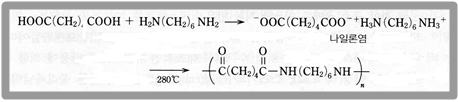
이에 비해 축합 고분자(condensation polymer)는 대부분 물이나 알코올과 같이 작은 분자가 제거된 다음 두 분자가 합쳐져 생성되는 고분자이다. 이렇게 반응하는 분자들 끝에는 카르복시기나 아민기와 같은 반응 가능한 작용기가 있다. 이러한 반응을 하기 위해서는 두 반응하는 분자가 서로 결합하여야 한다. 나일론의 예를 들면 다음과 같다. 이 반응에는 카르복시기와 아민기가 반응하여 에스테르 결합을 하게 된다.
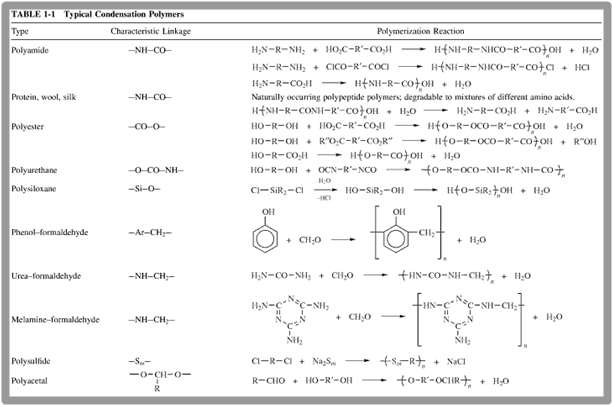
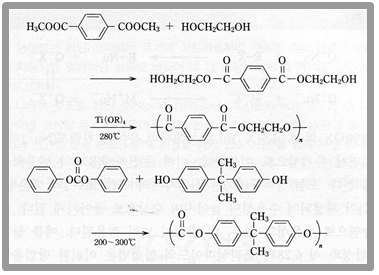
이러한 축합 중합을 하는 고분자의 예를 들면 다음과 같다.
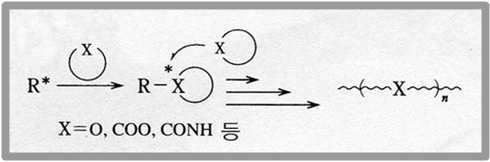
또한 이러한 중합 외에도 고리 모양 모노머의 고리가 열려 중합하는 개환 중합(ring-opening polymerization)이 있으며 개환 중합의 일반적인 과정은 다음과 같다.
사슬-성장 중합 반응에서 가장 많이 사용되는 단량체는 에텐(ethene)과 에텐의 네 수소중 하나가 치환된 치환체이다. 이렇게 하나가 치환된 에텐 치환체를 알파 올레핀(alpha olefin)이라고 하는데 이러한 단량체로부터 만들어진 고분자를 바이닐 고분자(vinyl polymer)라고 한다.
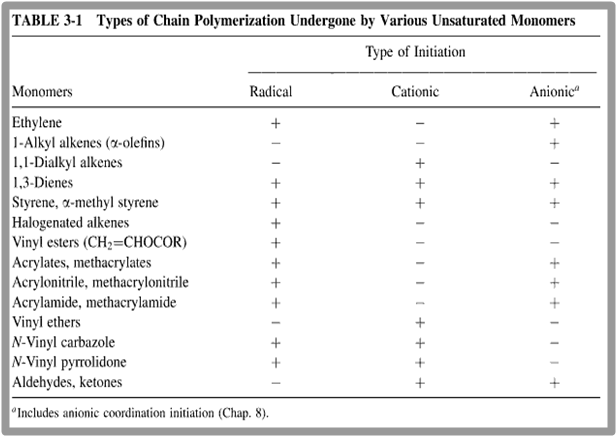
사슬-성장 중합 반응의 메커니즘은 라디칼 중합 반응(radical polymerization)과 양이온중합 반응(cation polymerization) 그리고 음이온 중합 반응(anion polymerization) 중 하나를 따른다. 이는 반응을 매개하는 것이 무엇이냐에 따른 분류이다. 다음 표는 각 단량체에 따른 반응 메커니즘의 종류이다. 이 세 반응 모두 중합 반응을 시작하는 개시 단계(initiation step), 반응이 진행되는 전파 단계(propagation step), 그리고 반응이 끝나고 사슬의 성장이 끝나는 종결 단계(termination step)가 존재한다.
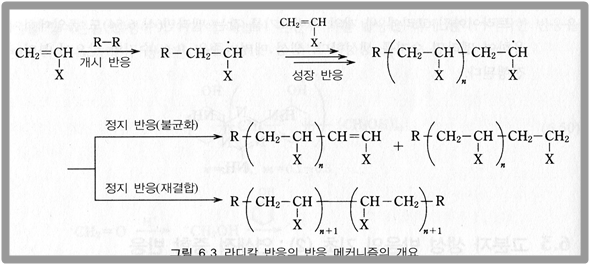
라디칼 중합 반응(radical polymerization)은 라디칼을 성장 말단으로 하는 중합 반응을 말한다. 또한 사슬-성장 중합 반응이 이 반응을 통해 진행되려면 라디칼이 단량체에 첨가되어 단량체 분자의 일부가 라디칼로 변하여야 한다. 라디칼 중합 반응의 메커니즘과 사슬-성장 반응을 간단히 나타낸 반응식은 다음과 같다.
여기서 I는 개시제, M은 모노머, P는 생성 고분자, A는 연쇄 이동제이다.
이렇게 알켄 단량체가 수백 수천 개 성장하는 사슬에 첨가되다가 라디칼이 반응하여 사라지게 되면 사슬 반응이 끝난다. 이렇게 전파 위치가 파괴되는 경우는 다음과 같다.
- 사슬 두 개가 전파 위치에서 서로 결합한다.
- 사슬 두 개 중 하나는 알켄으로 산화되고 다른 하나는 수소 원자가 자리를 옮겨 알케인으로 환원되면서 불균등화 반응(disproportionation)이 일어난다.
- 한 개의 사슬이 라디칼과 반응하는 불순물과 반응한다.
이렇게 전파 위치가 파괴되는 단계를 종결 단계라고 한다. 엄밀히 말하면 고분자 끝의 작용기는 다른 반복 단위와 다르므로 표시해야 하지만 고분자 전체 크기에 비해 매우 미미하므로 고분자의 물리적 성질에 거의 영향을 미치지 못하고, 따라서 일반적으로 표시하지도 않는다.
고분자의 분자량은 사슬 전달(chain transfer)이라는 과정으로 조절할 수 있다. 성장하는 사슬이 분자 XY와 반응하여X•가 사슬을 종결시키고 Y•가 새 사슬을 형성하면 된다. 이 때 용매, 라디칼 개시제, 균일 분해될 수 있는 결합이 있는 분자 등이 XY로 쓸 수 있다.
일치환 에틸렌이 사슬-성장 중합반응을 하면 입체 장애(steric hinderance) 때문에 전파가 이루어지는 위치가 알켄에서 치환되지 않은 탄소에서 일어나기 쉽고 따라서 한 단량체의 머리 부분이 다른 단량체의 꼬리 부분에 연결되는 머리-꼬리 첨가 반응(head-to-tail addition)이 잘 발생한다. 그러면 두 탄소마다 일정하게 치환기가 있는 고분자가 생기게 된다. 만약 치환기가 크고 페닐과 같이 안정화가 잘 되는 것이라면 라디칼이 쉽게 안정화되므로 머리-꼬리 첨가반응이 잘 일어난다.
그렇지만 반대로 치환기가 작아 입체 장애가 심하지 않고 라디칼이 잘 안정화되지 않는다면 머리-머리 첨가반응이나 꼬리-꼬리 첨가반응이 발생하기도 한다. 특히 치환기가 플루오린(F)일 때 이러한 반응이 잘 일어난다. 그렇지만 그렇더라도 이런 첨가반응은 전체사슬의 1/10도 되지 않는다.
알켄을 라디칼로 만들 수 있을 정도로 매우 강력한 라디칼을 생성할 수 있는 균일 분해반응을 쉽게 하는 화합물은 모두 라디칼 중합 반응의 개시제로 사용할 수 있다. 이러한 개시제의 공통점은 결합이 비교적 약해 균일 분해가 잘 일어난다는 것이다. 개시제의용해도와 중합 반응이 일어나는 온도 두 가지를 고려하고 라디칼 개시제를 골라야 한다. 예를 들어 과망간산칼륨(potassium permanganate)는 수용성 개시제가 필요할 때 쓰이고 고온 반응을 위해서는 고온에서도 안정한 삼차-뷰톡시(tert-butoxy) 라디칼을 쓰게 된다.
만약 전파 위치가 사슬의 수소와 반응하면 수소가 떨어져 나가고 그 자리에 가지가 생길 수 있다. 만약 사슬 끝에 있는 수소가 제거되면 짧은 가지가 만들어지고 사슬 중간에 있는 수소가 제거되면 긴 가지가 생긴다. 둘 모두 가능성이 있으나 사슬 끝이 더 접근하기 편하므로 긴 가지보다는 짧은 가지가 더 많이 생긴다. 일반적으로 가지가 많으면 많을수록 고분자의 밀도가 낮아지므로 가지가 적은 선 모양의 플라스틱은 비교적 단단해지고 가지가 많은 플라스틱은 유연해진다.
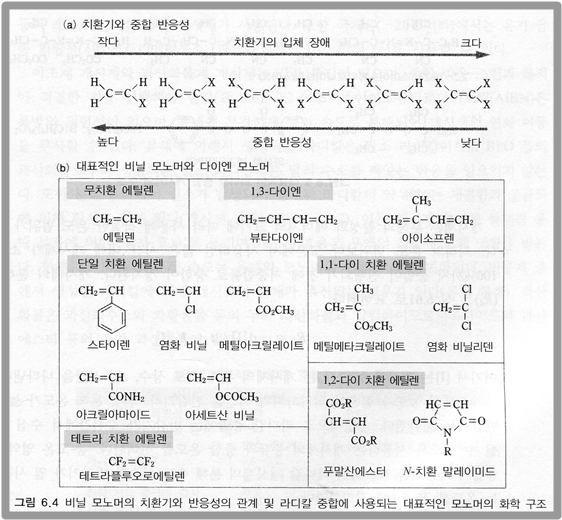
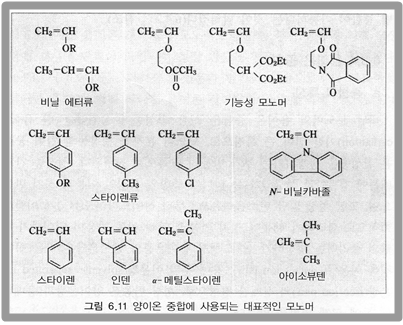
이렇게 비닐 모노머의 중합 반응성은 반응하는 이중 결합에 직접 결합하는 치환기의 종류와 위치, 수에 따라 크게 변화하는데, 이러한 비닐 모노머의 치환기와 반응성의 관계 및 라디칼 중합에 사용되는 대표적인 모노머의 화학 구조는 아래 도표와 같다.
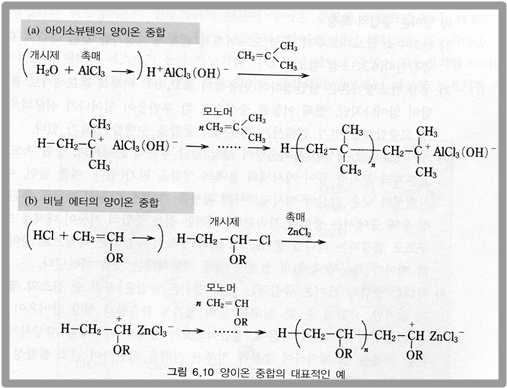
양이온 중합 반응은 연속적 중합 반응 중 양이온을 성장 말단으로 하는 중합을 말한다. 양이온 중합 반응의 매커니즘과 대표적인 예는 다음과 같다.
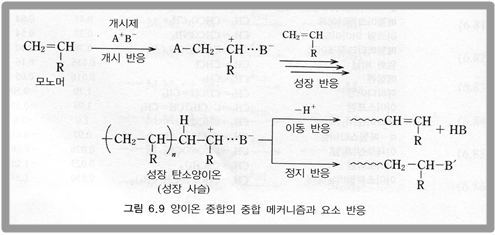
이러한 반응에서 가장 널리 쓰이는 개시제는 탄소양이온을 생성하는 산성 화합물이나 양이온이며 할로젠화 알킬과 같은 탄소 양이온원과 루이스산도 자주 쓰인다. 이 때 탄소 양이온원으로부터 양이온 생성을 루이스산이 촉진하는 것으로부터 양이온원을 개시제, 루이스산을 촉매라 하며 이들의 조합을 개시제원이라고 한다.
개시제는 수소가 더 많이 결합한 sp2 탄소에 첨가된다. 그렇게 계시 단계에서 생성된 양이온이 두 번째 단량체와 반응하여 새 양이온이 생성되고 이 새 양이온은 다시 세 번째 단량체와 반응하게 된다. 이와 같이 계속해서 단량체가 사슬에 첨가되면 새로운 양전하의 전파 위치는 바로 가장 나중에 첨가된 단량체의 끝에 위치하게 된다. 이렇게 전파된 반응은 양성자가 손실되거나, 친핵체(nucleophile)이 전파 위치에 첨가되거나, 용매와 사슬-전달 반응이 일어나게 되면 종결된다.
양이온 중합 반응 동안에 생성된 탄소 양이온 중간 생성물은 다른 탄소양이온과 마찬가지로 자리를 옮겨서 더 안정한 탄소양이온이 생성될 수 있으면 1,2-수소음이온 옮김(1,2-hydride shift)나 1,2-메틸 옮김(1,2-methyl shift)에 의해 자리 옮김(rearrangement)을 할 수 있다. 또한 양이온 중합 반응을 잘 할 수 있는 알켄은 하이퍼콘쥬게이션(hyperconjugation)이나 공명에 의해 전자를 주므로 전파 위치의 양전하를 안정화시킬 수 있는 치환기가 있는 단량체들이 양이온 메커니즘에 의해 중합 반응이 가장 잘 진행된다.
양이온 중합의 주요 특징은 다음과 같다.
탄화수소 모노머로부터 극성 모노머까지 전자 공여성기를 갖는 다수의 모노머가 중합한다.
성장하는 탄소 양이온은 불안정하므로 반응성이 크고 0도 이하에서도 반응이 빠르지만 자리 옮김과 같은 연쇄 이동을 중심으로 한 부반응(side reaction)이 일어나기 쉽고 고중합체를 얻으려면 저온에서 중합해야만 하는 단점이 있다. 때문에 경제적으로 불리하므로 실제 공업에선 다른 반응보다는 적게 쓰인다.
개시제로부터 생성된 음이온쌍이 성장 말단 부근에 존재하고 중합 속도와 생성 고분자의 분자량 등이 개시제와 용매의 영향을 받기 쉽다. 따라서 모노머에 다라 중합 과정이 달라지는 라디칼 중합과는 다르며 양이온 중합이 개시제(촉매)의 설계에 따라 제어 가능하게 된다.
라디칼 중합과 음이온 중합과는 달리 양이온 중합은 공기 중 산소의 영향을 받지 않으나 중합계 중 물이나 알코올 등의 염기성 불순물과 성장 양이온이 연쇄 이동과 정지를 일으키므로 보통 중합의 재현성을 향상하기 위해 수분을 잘 제거하고 정제된 시약을 사용해 건조한 불활성 기체 내에서 반응시킨다.
양이온 중합에 사용되는 대표적인 모노머의 예를 들면 위 그림과 같다. 탄소 양이온을 중간체로 하므로 친전자 반응에 적합한 모노머가 쓰인다.
음이온 중합 반응에서는 게시제가 친핵체(nucleophile)로서 알켄과 반응하여 음이온인 전파 위치를 생성하게 된다. 알켄 자체가 이미 전자가 풍부한 이상 친핵체는 알켄과 쉽게 반응하지 못한다. 따라서 개시제가 소듐 아마이드(sodium amide)나 뷰틸리튬(butyllithium)과 같이 매우 좋은 친핵체여야 반응이 일어난다. 그리고 알켄에도 전자 밀도를 감소시킬 수 있는 치환기(electron-withdrawing effect가 가능한 치환기)가 있어야 한다. 이렇게 모노머 분자가 중합하는 분자의 친핵 공격을 받아 계속 부가 반응이 반복되고 성장하는 분자 간의 정전기적 반발 때문에 다시 결합하거나 불균일화되지 않은 라디칼 중합과 같은 이분자 정지 반응이 일어나지 않으며 하이드라이드(H-)가 성장 말단으로부터 잘 이탈하지도 않으므로 열역학적으로 불리해 정지 반응과 연쇄 이동 반응도 잘 일어나지도 않는다.
만약 용매와 사슬 전달 반응을 하거나 반응물 중의 불순물과 반응하면 반응이 종결된다. 만약 용매가 사슬을 종결할 수 있는 양성자를 줄 수 없거나 탄소음이온과 반응을 할 수 있는 불순물을 완전히 제거하게 되면 모든 단량체가 반응할 때까지 사슬-전파 반응이 계속된다. 따라서 전파 위치는 여전히 활성 상태이므로 단량체를 첨가하면 중합 반응은 계속될 것이다. 이러한 사슬을 활성 고분자(living polymer)라고 한다. 활성 고분자는 양이온 중합 반응과는 달리 고분자로부터 양성자가 손실되어 사슬이 종결될 수 없거나 라디칼 중합 반응과는 달리 불균등화나 라디칼 재조합으로 인해 사슬이 종결될 수 없어 보통 음이온 중합 반응으로 생성된다.
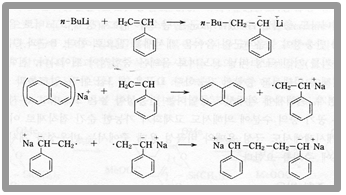
음이온 중합의 대표적인 개시제와 모노머는 다음과 같다.
또한 개시 반응의 예를 들면 다음과 같다. 다음은 스타이렌의 중합 반응이다.
알켄의 치환기에 따라 사슬-성장 중합 메커니즘이 라디칼인지, 음이온인지, 양이온인지가 달라진다. 라디칼을 안정화시킬 수 있는 치환기가 있으면 라다칼 중합 반응을 하고 양이온을 안정화시킬 수 있으면 양이온 중합반응, 음이온을 안정화시킬 수 있으면 음이온 중합반응을 한다. 물론 이렇게 한 가지 반응 경로로만 중합이 일어나는 것은 아니다. 예를 들면 스타이렌(styrene)은 페닐기가 벤질 라디칼, 벤질 양이온, 벤질 음이온 모두를 안정화시킬 수 있으므로 모든 반응 경로가 가능하다. 이 때 중합 반응은 반응을 시작할 때 선택하는 개시제의 성질에 따라 달라지게 된다.
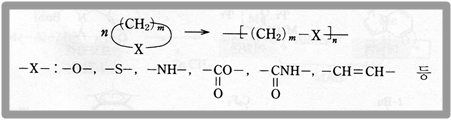
에틸렌과 치환 에틸렌들이 사슬-성장 중합 반응에 가장 일반적으로 쓰이는 단량체이지만 다른 화합물을 중합시키는 것도 가능하다. 예를 들면 에폭사이드(epoxide)도 사슬-성장 중합 반응이 가능하며 이러한 방식으로 고리 화합물의 고리가 열려 고분자를 만드는 것을 개환 중합(ring-opening polymerization)이라고 한다. 개환 중합의 일반식은 다음과 같다.
개시제로 HO-나 RO-와 같은 친핵체가 사용되면 음이온 메커니즘에 의해 중합 반응이 발생한다. 친핵체가 에폭사이드의 입체 장애가 적은 탄소를 공격할 수 있기 때문이다. 또한 개시제가 루이스산이나 양성자를 제공할 수 있는 산인 경우 에폭사이드는 양이온 중합 반응을 한다. 특히 산 조건하에서는 친핵체가 에폭사이드의 치환이 많이 된 탄소를 공격하게 된다. 이처럼 개환 중합에도 양이온 중합과 음이온 중합이 가능하며 때로 배위 중합이나 라디칼 중합을 하기도 한다.
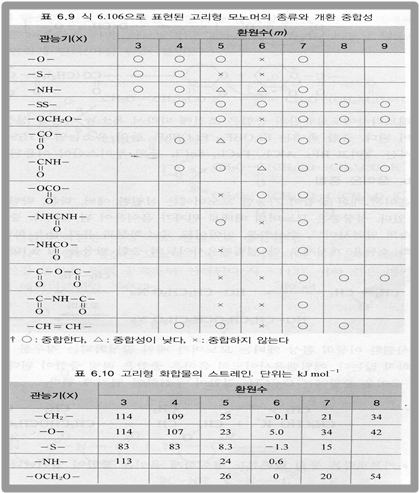
개환 중합의 대표적인 모노머의 종류와 개환 중합성은 다음 표와 같다.
단계-성장 고분자(step-growth polymer)는 두 개의 작용기가 있는 분자들 간의 반응에 의해 만들어진다. 작용기들이 반응할 대 대부분 물(H2O)이나 알코올(ROH), 염화수소(HCl)와 같은 작은 분자가 제거된다. 따라서 이러한 고분자를 축합 고분자(condensation polymer)라고 하기도 한다.
이러한 고분자에는 다음 두 종류가 있다.
화합물에 A와 B 같이 서로 다른 두 개의 작용기가 반응하여 생성되는 고분자
이작용기 화합물(bifunctional compound) 두 개가 서로 반응해 생성되는 고분자
사슬-성장 고분자와 달리 단계-성장 고분자는 사슬 반응을 통해서는 만들어지지 않는다. 사슬 반응과는 달리 반응이 절반 정도 진행되어도 반응 생성물은 거의 이량체(dimer)나 삼량체(tirmer)이다. 이는 단계-성장 중합 반응으로 긴 사슬을 만들려면 수율이 매우 좋아야 한다는 의미이다.
이러한 단계 중합은 세 가지 방법이 있다. 먼저 폴리에틸렌테레프탈레이트(polyethylene threphthalate, PET)와 같은 폴리에스터나 나일론 66과 같은 폴리아마이드(polyamide)가 만들어지는 방법인 중축합(polycondensation)이 있다.
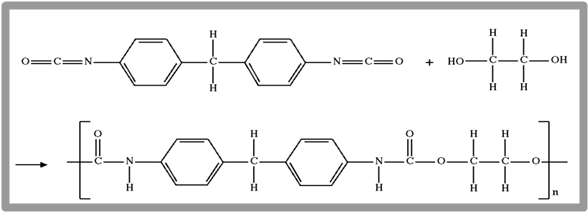
이렇게 축합 반응이 반복되어 중합이 진행되는 중축합외에도 부가 반응의 반복되어 중합하기도 하는데 이를 중부가(polyaddition)라고 하며 대표적인 고분자로 폴리우레탄(polyurethane)이 있다. 폴리우레탄의 합성 반응은 다음과 같다.
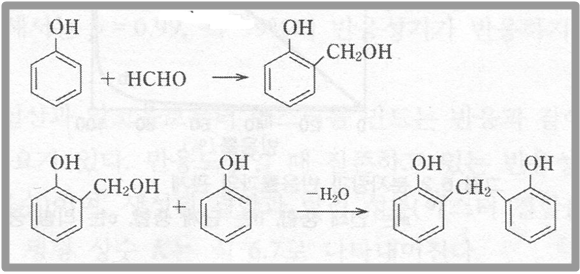
그리고 페놀 수지나 멜라민 수지와 같이 부가 반응과 축합 반응이 섞인 부가 축합도 있다. 페놀 수지는 페놀과 포름알데히드가 부가 반응하고 이 생성물이 축합 반응하여 생성된다. 다음 반응에서 위 반응은 부가 반응이고 아래 반응은 축합 반응이다.
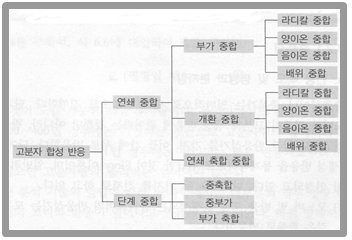
따라서 고분자 합성 반응을 정리하면 다음과 같다.
이처럼 고분자 합성법은 매우 다양하며 연쇄 중합과 단계 중합에 따라 구분할 수 있다. 그렇지만 점차 다양한 고분자 합성법이 발견되어 산업 현장에서 유용하게 쓰이고 있다. 이러한 합성법으로는 Ziegler-Natta 촉매를 이용한 합성법, 복분해를 이용한 방법, 그리고 그룹 트란스퍼(group transper), 앞에서도 잠깐 언급했지만 ‘리빙 양이온(living cation)’을 이용한 방법, 고분자 치환 방법 등이 있다. 이러한 방법의 장단점을 요약하면 다음과 같다.
이렇게 한 가지 종류의 단량체가 반응을 하는 동종중합체(homopolymer)외에도 단량체 두 종류 이상이 고분자를 형성할 수 있는데, 이런 고분자를 공중합체(copolymer)라고 한다. 공중합체를 형성하는 여러 단량체의 수가 늘어나면 그 단량체들이 만들 수 있는 다른 공중합체의 수가 매우 빨리 증가한다. 두 종류의 단량체만으로도 각 단량체의 양을 조절하게 되므로 성질이 서로 다른 공중합체를 만들 수 있다. 사슬-성장 고분자와 단계-성장 고분자 모두 공중합체가 되는 것이 가능하다.
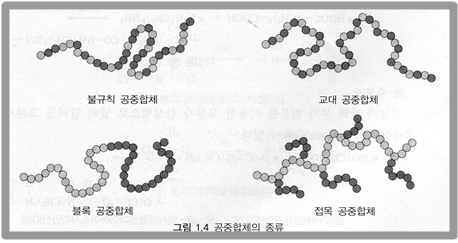
공중합체에는 네 종류가 있다. 이렇게 다양한 구조가 가능하므로 공중합체를 다양하게 설계할 수 있고, 따라서 성질 또한 다양하게 만들 수 있게 된다.
교대 공중합체(alternating copolymer)는 두 개의 단량체가 교대로 이어진다.
블록 공중합체(block copolymer)는 각 종류의 단량체가 블록을 형성한다.
불규칙 공중합체(random copolymer)는 단량체의 분포가 불규칙적이다.
접목 공중합체(graft copolymer)는 하나의 단량체로 형성된 주 사슬에 다른 단량체로 형성된 가지가 접목되어 있다.
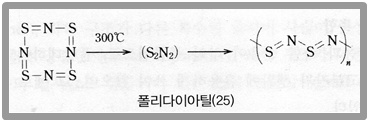
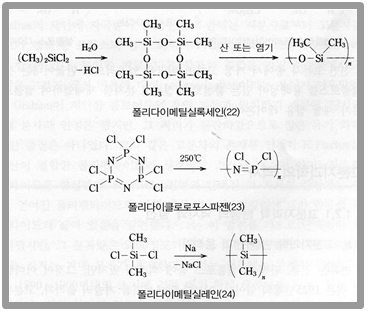
또한 주 사슬이 탄소 외에도 규소(Si), 인(P), 황(S), 산소(O), 질소(N) 등 비금속 원소로 이루어질 수도 있다. 예를 들어 폴리실록세인은 규소와 산소 간의 단일 결합으로, 폴리포스파젠은 질소와 인 간의 이중결합으로 이루어져 있다. 이들은 모두 유리 전이 온도가 낮아 주로 합성 고무로 쓰인다. 그 외에도 규소 결합만으로 이루어진 폴리실레인이나 배위 결합이 주 사슬에 있는 고분자도 있다. 또한 인과 질소 결합으로 이루어진 폴리다이아틸은 저온에서 초전도성이 있다.
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기