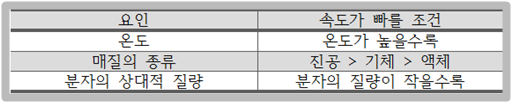
기체의 확산 속도에 영향을 주는 요인은?
[기체의 확산]
확산이란 어떤 물질 속에 이종의 물질이 점차 섞여 들어가는 현상을 말하는데, 예를 들어 컵의 물에 잉크를 한 방울 떨어뜨리면 시간이 지남에 따라 잉크가 퍼져 전체가 균일하게 섞이는 것을 말한다. 이와 같은 현상은 기체와 기체 사이에서도 볼 수 있고, 때로는 기체와 고체, 액체와 고체 사이에서도 일어난다.
[기체의 확산 속도]
(1) 온도가 높을수록
기체 분자의 운동 에너지를 구해 보면
(2) 매질의 종류에 따라
아무리 분자 자체의 속도가 빠르다고 하더라도 그것을 방해하는 다른 분자가 촘촘하게 존재하면 확산 속도는 느려지게 된다. 따라서
- 진공 : 방해가 없으므로 운동 속도 자체가 확산 속도가 되고
- 기체 속 : 기체의 틈새를 피해서 확산되어야 하므로 진공에 비해서 느릴 것이며,
- 액체 속이라면 기체에 비해 분자의 틈새가 비좁으므로 더욱 느려질 것이다.
(3) 분자의 질량이 작을수록
똑같은 온도 조건에서 질량이 작을수록 분자의 운동이 활발하므로 확산 속도가 빠르다.
예) 염화수소 분자보다 암모니아 분자의 질량이 작으므로 암모니아 분자의 확산 속도가 더 빠르다.
[그레이엄의 법칙 (Graham's law)]

일정한 온도와 압력 상태에서 기체의 확산 속도는 그 기체 분자량의 제곱근(밀도의 제곱근)에 반비례한다는 법칙이다. 같은 온도에서 기체 분자의 운동에너지는 그 종류와는 관계없이 일정하므로 가벼운 분자는 빨리 움직이고, 무거운 분자는 느리게 운동한다. 온도가 같으므로 그들의 평균 분자 운동에너지는 같다.
곧, 용기 안에 있는 등온 ·등압의 기체가 용기 벽에 뚫린 작은 구멍을 통해 유출할 때, 그 속도는 기체 밀도의 제곱근에 반비례하고, 용기 내외의 압력 차의 제곱근에 비례한다. 또한 일정한 온도에서 일정량의 기체 분자가 용기의 벽에 자주 부딪치므로 단위 시간당 충돌 횟수가 증가하여 압력이 커진다. 용기 안의 압력이 높을수록 용기 속의 기체가 빠르게 밖으로 나가게 된다. 용기 내외의 압력을 각각 p1, p2, 기체의 밀도를 ρ, 단위시간에 유출하는 기체의 속도를 v라 하면 속도 v는
그레이엄의 법칙을 통해 확산속도의 비를 구할 수 있는데, 다음과 같다.
Q. 표준상태에서 산소의 밀도는 1.429g/L, 이산화탄소의 밀도는 1.964g/L이다. 어떤 원소가 얼마나 더 빠르게 확산하는가? 느린 확산속도를 1로 잡으면 확산속도 법칙을 다음과 같이 쓸 수 있다. |
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기