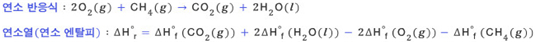엔탈피와 엔트로피에 대해 설명해보세요.
[엔탈피 (enthalpy)]
엔탈피는 에너지와 유사한 성질의 상태함수이다. 엔탈피는 에너지의 차원을 가지고 있는데 계가 지나온 과정에 관계없이 온도, 압력, 그 계의 조성에 의해서만 결정되는 값이다. 기호로 표시해보면 H=E+PV 이다. 엔탈피 H는 내부 에너지 E에 압력 P와 부피 V의 곱을 더한 값이다. 에너지 보존법칙에 의하면 내부 에너지의 변화량은 계에 가해진 열량에서 계에 의해서 수행된 일의 양을 뺀 것과 같은 값이다.
만일 일정한 압력 하에서 부피의 변화에 의해서만 일이 수행되었다면 엔탈피의 변화는 계에 가해진 열량과 같은 값이 된다. 다른 에너지 함수에서와 같이 엔탈피의 절대값을 아는 것은 쉬운 일이 아니며 꼭 필요한 것도 아니다. 각 물질에서 엔탈피가 0인 상태를 기준 상태로 하여 편리하게 이용할 수 있다.
[엔트로피 (entropy)]
무작위 또는 무질서의 상태를 의미한다. 즉 시스템을 그냥 내버려두면 언젠가 엔트로피가 최대 수준까지 증가해 그 시스템은 기능을 정지하거나 해체되어 버리고 만다는 것이다. 따라서 어떤 시스템이 계속 주어진 목적을 달성할 수 있기 위해서는 엔트로피의 증가를 억제하는 활동 또는 입력이 반드시 필요하게 되는데, 이를 부의 엔트로피라고 한다.
[엔탈피에 대하여]
내부 에너지를 U, 압력을 p, 부피를 V라고 할 때, 엔탈피 H는 H=U+pV로 표시할 수 있다.
여기서, 엔탈피는 J.W.깁스에 의한 열함수, 열함량에 해당되고, 화학의 열함량, 열공학에서는 전열량이라고 하기도 한다. 만일 시스템의 압력이 일정한 상태인 경우에는, 시스템에 출입한 열량은 그 시스템의 엔탈피 변화와 같게 된다. 또 엔탈피 변화는 근본적으로 경로에 의존하지 않는 상태함수다. 이와 같은 특성으로, 엔탈피는 기화, 액화, 승화 등의 다양한 상태변화까지 편리하게 표현 할 수 있다.

그러나 물질이 가지는 고유한 내부에너지를 알 수 없기에 절대 엔탈피의 양은 알 수 없지만, 물질 변화가 일어날 때의 엔탈피 변화량에 관심을 갖게 되었으며, 이것은 열량계를 이용하여 측정 가능하고 화학 결합의 상대적 세기, 서로 다른 원자들의 특성, 특정 반응이 일어날 수 있는지 등을 설명하는 데 쓰일 수 있는 유용한 정보이다.
엔탈피는 조건에 따라 그 양이 달라지기 때문에 그 변화량을 정확하게 비교하려면 압력, 온도, 물리적 상태 등의 조건이 분명하게 제시되어 있어야 한다. 그러나 조건을 명확히 제시한다 하더라도 그 조건이 다르다면 엔탈피 변화량을 비교하기가 쉽지 않다. 그래서 엔탈피 변화량을 나타낼 때의 조건을 통일적으로 정해 이를 표준상태로 삼아 사용하기로 하였다.
표준상태는, 온도는 특별한 언급이 없는 한 25℃(298.15K), 압력은 1기압, 용액의 경우에는 농도 1몰/L, 물리적 상태는 25℃에서 가장 안정한 상태로 정하였다. 표준 상태에서의 엔탈피 변화를 표준 엔탈피 변화라고 하며, 기호 △HT° 로 나타내는데 아래 첨자 T는 엔탈피를 제시한 온도이다. 온도를 나타내지 않은 경우는 25℃(298.15K)인 때이다.
Q. A상태 물질이 내부에너지 100, 압력 2, 부피 60으로 존재할 때, 엔탈피는? A. 엔탈피= 100 + 2 * 60 = 220 (그러나, 내부에너지는 알 수 없기에 단순히 상태에 대한 엔탈피는 구할 수 없음. 현실적으로는 표준엔탈피를 기준으로 해서 상대적으로 달라진 엔탈피 변화값을 구함) |
1기압 하에서 일어나는 반응의 엔탈피 변화량을 특별히 표준 반응 엔탈피라 부르고, ΔHor로 나타낸다. 이는 이 반응에서 출입하는 열량을 측정하면 바로 구할 수 있다. 압력이 일정한 과정에서 화학 반응의 반응 엔탈피는 생성물의 엔탈피 값과 반응물의 엔탈피 값의 차이이다.
만약 반응물과 생성물의 엔탈피 값을 알고 있다면, 우리는 직접 실험하지 않고도 반응 엔탈피를 계산할 수 있다. 즉 반응에서 출입하는 열량을 직접 실험하지 않고, 계산으로도 구할 수 있다.
그러나 실험적으로 구할 수 있는 것은 엔탈피의 절대값이 아니라 변화이다. 따라서 변화량을 표현할 어떤 기준이 필요하며, 이 기준점으로부터 각 화합물의 엔탈피 값을 상대적인 값으로 나타낸다. 이렇게 나타낸 값이 표준 생성 엔탈피(ΔHof)이다. 이는 마치 산의 높이를 비교하기 위해 해수면이라는 기준을 잡고, 해발고도로 표현하는 방식과 같다.
1기압에서 어떤 화합물 1몰이 그 화합물을 구성하고 있는 성분 원소의 가장 안정한 상태에서 생성될 때의 반응 엔탈피를 그 화합물의 표준 생성 엔탈피라 하는데, 이를 표준 생성열이라 부르기도 한다. 이와 같은 ΔHof 의 정의는 1기압에서 안정한 원소들의 ΔHof 값을 모두 0로 하고, 화합물들의 ΔHof 값을 정하는 것과 같다. 예로, 열역학적으로 안정한 원소 상태는 탄소는 흑연이고, 수소와 산소는 각각 기체 상태의 H2(g)와 O2(g)이며, 이들의 ΔHof 값은 모두 0이다.
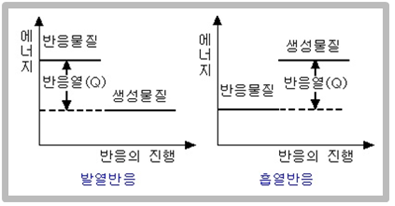
흔히 화학에서는 반응을 흡열반응과 발열반응으로 구분한다. 흡열반응은 반응에 의해 온도가 낮아지는 경우이다. 소금을 물에 녹이면 온도가 약간 내려가는 것이 이의 예이다. 이는 반응 후의 온도를 반응 전의 처음 온도와 같게 하기 위해서는 주위에서 열을 흡수해야 함을 의미한다. 따라서 QP>0 이므로 엔탈피는 증가한다.
이와 반대로, 발열반응은 물과 황산을 섞을 때나 연료가 탈 때처럼 반응에 의해 계의 온도가 올라가는 경우이다. 이때는 반응 후의 온도를 반응 전과 같게 하기 위해서 열을 방출시켜야 한다. 즉 QP<0 가 되고, 따라서 엔탈피는 감소한다. 즉 흡열 반응에서는 엔탈피가 증가하고, 발열 반응에서는 엔탈피가 감소한다.
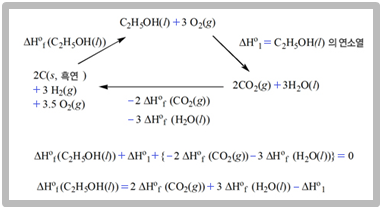
이산화탄소 (CO2(g))와 물(H2O(l))처럼 구성 원소로부터 그 화합물을 직접 생성시키는 것이 용이한 경우는, 생성 반응열을 측정하여 그 화합물의 ΔHof 값을 구한다. 그러나 에탄올(C2H5OH(l))처럼 원소에서 직접 그 화합물을 생성하는 것이 어려운 경우는 간접적인 방법으로 그 화합물의 ΔHof 값을 구한다. 이때에는 여러 단계를 거쳐 처음 상태로 되는 순환 과정에서 ‘각 단계의 엔탈피 변화량의 합은 0’이라는 헤스(Hess)의 법칙을 이용하면 된다.
이런 방법으로 많은 화합물의 ΔHof 값들을 구해서 문헌에 표로 정리되어 있다. 이를 이용하여 화학반응의 반응 엔탈피(반응열)을 실험하지 않고도 구할 수 있다.
반응 엔탈피는 생성물들의 ΔHof 값의 합에서 반응물의 ΔHof 값의 합을 빼서 구하는데, 이때 반응식의 계수도 고려되어야 한다. 예로 1기압에서의 메탄 기체(CH4(g))의 연소 반응에서 연소열(연소 엔탈피)은 다음과 같이 구할 수 있다.
O2(g)는 안정한 원소이므로 이의 ΔHof 값은 0임을 상기할 필요가 있다.
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기