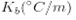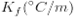총괄성이란 무엇인가요?
[용액의 총괄성 (colligative property, 속일성)]
화학에서 입자(분자나 원자)의 성질에 관계없고 입자의 수에 따라 변하는 물질의 성질.
이상기체의 압력, 용매 속에 녹아 있는 입자에 의한 용매의 어는점 내림 등이 그 예이다.
용질과 용질 사이, 용매와 용매 사이, 용매와 용질 사이의 인력이 동일한 용액을 이상 용액이라고 하는데, 이 이상 용액에서 '용액의 총괄성'이 성립한다. 이상용액의 조건을 만족하게 되면, 용질의 종류에는 상관없이 용질의 양(농도)에 따라서 용액의 성질이 결정되게 되는데, 이는 다음의 네 가지 특성의 원인이 된다.
- 순수한 용매에 대한 비휘발성 용질이 용해된 용액의 증기압 내림
- 끓는점 오름
- 어는점 내림
- 삼투압 현상
이를 용액의 총괄성이라 부르며, 용질의 종류에 상관없이 농도에만 의존하는 용액의 특성 값들이다.
(1) 순수한 용매에 대한 비휘발성 용질이 용해된 용액의 증기압 내림
증발은 용매, 혹은 용액의 표면에서 일어난다. 증기압이란, 어떤 온도에서 용매의 기화<->액화 현상이동적 평형 상태를 이룰 때의 증발된 용매가 나타내는 압력이다. 증발은 용매가 기화되는 현상이기 때문에, 용액은 순수한 용매에 비하여 비휘발성 용질이 용해된 용액은 표면에 용질 입자가 존재하는 만큼 증발이 줄어들어, 결국 증기압이 낮아지게 된다. 이 현상이 증기압 내림이며, 증기압 내림의 효과를 식으로 나타내어 보면,
비휘발성 비전해질 용액의 증기압은 순수한 용매의 증기압보다 항상 낮다. 증기압 내림(ΔP)을 증발 속도와 응축 속도로 설명하면, 순수한 용매의 일정 온도 평형 상태에서의 두 속도는 같다. 비휘발성 용질을 가하면 표면에 존재하는 용매 분자 수가 감소하여 증발 속도가 감소한다. 평형에 도달하기 위해서는 응축 속도도 감소해야 하며, 그러기 위해서 증기압이 낮아져야 한다. 증기압이 낮아지는 정도를 라울의 법칙(Raoult's law)으로 알 수 있다.
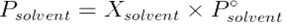
라울의 법칙은 용매의 증기압(
(참고) 몰분율(mole fraction, X)이란
총 몰수에 대한 용질의 몰수의 비이다. 몰 백분율은 몰분율에 백을 곱한 것이다.
몰분율 = 용질의 양(몰수) / [용질의 양(몰수)+용매의 양(몰수)]
몰백분율(mol %) = 몰분율 X 100
(2) 끓는점 오름
용매 | 끓는점( oC) | |
아세트산 | 117.9 | 30.7 |
벤젠 | 80.1 | 2.53 |
이황화탄소 | 46.2 | 2.34 |
사염화탄소 | 76.5 | 5.03 |
클로로폼 | 61.7 | 3.63 |
디에틸에테르 | 34.5 | 2.02 |
에탄올 | 78.5 | 1.22 |
물 | 100.0 | 0.512 |
▲ 여러 용매들의 끓는점과 끓는점 오름 상수
용액은 언제나 순수한 용매보다 높은 온도에서 끓는다. 액체의 끓는점은 증기압이 외부 압력과 같아지는 온도이다. 그런데, 모든 온도에서 용액의 증기압은 순수한 용매의 증기압보다 낮다. 물론, 용매의 끓는점에서의 용액의 증기압은 외부압력보다 낮다.
그렇기 때문에 그 온도에서 용액은 끓지 않는다. 온도를 더 높여야 용액의 증기압이 외부 압력과 같아지고 끓기 시작한다. 이렇게 용액의 끓는점이 순수한 용매의 끓는점보다 높은 것을 끓는점 오름(boiling point elevation,
증기압 내림과 마찬가지로 끓는점 오름의 정도도 용질 입자의 농도에 비례한다.
끓는점 오름의 현상은 증기압 내림의 설명으로부터 이해할 수 있다. 특정 온도에서 용액의 증기압이 내려간다는 것은, 순수한 용매의 끓는점에서의 증기압이 1기압이 되지 못한다는 것이다. 이 뜻은, 온도가 기존 끓는점보다 더 높아야 용액의 증기압이 1기압이 되고, 용액이 끓을 수 있다는 의미이다. 끓는점 오름의 식은 다음과 같이 나타난다.
이 때,
(참고) 몰랄농도 (molality,
몰랄농도는 용매 1000g에 녹아있는 용질의 몰수로 정의되며,
몰랄농도(
몰랄농도는 용액의 양이 아닌 용매의 양임을 주의해야 한다.
(3) 어는점 내림
용매 | 끓는점( | |
아세트산 | 16.6 | 3.90 |
벤젠 | 5.5 | 4.90 |
이황화탄소 | -111.5 | 3.83 |
사염화탄소 | -23 | 3.00 |
클로로폼 | -63.5 | 4.70 |
디에틸에테르 | -116.2 | 1.79 |
에탄올 | -117.3 | 1.99 |
물 | 0.0 | 1.86 |
▲ 여러 가지 용매에 대한 상수의 값
물질이 얼 때, 오직 용매 분자만 고체를 형성하고 용질 분자들은 그것을 방해한다. 따라서 순수한 용매에 비해 어는점이 내려간다. 용액의 어는점은 용액의 증기압이 순수한 용매와 같아지는 온도이다. 그런데, 모든 온도에서 용액의 증기압은 용매의 증기압보다 낮으므로 용액은 용매보다 더 낮은 온도에서 언다. 이것을 어는점 내림(freezing point lowering,
어는점의 정의 또한, 화학적으로 해석하여 보면 용액의 증기압과 용액의 고체상태의 증기압이 같아지는 순간이라고 볼 수 있다. 이 때, 용액의 고체 상태는 순수한 용매만으로 이루어지므로 온도에 따른 증기압 곡선이 그대로이고, 용액은 온도에 따른 증기압 곡선이 y축의 음의 방향으로 이동한 모양이기 때문에 마찬가지 원리로 이번에는 용액에서 어는점이 낮아지게 된다. 이를 식으로 나타내면
(4) 삼투압
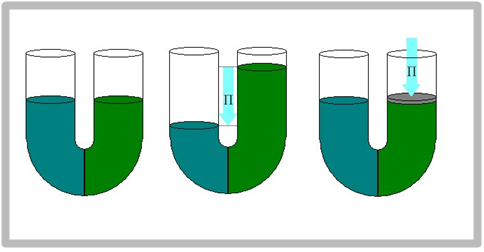
삼투압이란 농도가 다른 두 용액이 용매 분자만을 통과시키고 용질 분자는 통과시키지 않는 반투막(semipermeable membrane)으로 분리되어 있을 때, 농도가 낮은 쪽의 용매 분자들이 농도가 높은 쪽으로 이동해가는 것을 말한다. 삼투 현상은 반투막이 있을 때 평형으로 가는 과정이다. 반투막이 없다면 용질이 이동하여 평형을 이루겠지만, 이게 반투막에 의하여 불가능하니 용매가 이동하게 되는 것이다. 이 때, 반투막 사이의 압력은 삼투압으로 표현이 되는데, 삼투압의 식은 Π = CRT 로 나타난다.
U자 관 가운데에 반투막이 있어 순수한 용매(파란색)와 설탕 용액(초록색)을 분리하고 있는 것을 상상해보자. 용매인 물 분자는 반투막의 어느 방향으로든 자유롭게 움직이지만, 크기가 큰 설탕 분자들은 반투막을 통과하지 못한다.
용액 쪽의 반투막에는 용질 분자들이 용매가 막에 접촉하는 횟수를 줄게 하여, 용액 쪽에서는 나가는 물 분자보다 들어오는 물 분자의 양이 많게 된다. 이렇게 용액 쪽으로 물의 알짜 흐름으로 용액의 부피가 증가하고, 농도가 감소하게 된다.
용액의 높이가 높아질수록, 용매의 높이가 낮아질수록 두 높이 차에 의해 나타나는 압력의 차이는 용매 분자들을 용액 쪽에서 용매 쪽으로 밀어낸다. 나가는 양과 들어오는 양이 같아지는 평형에 도달하게 된다. 이 평형에서의 압력 차이를 삼투압(Osmotic pressure,
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기