고분자의 대표적인 특징을 말해 보십시오.
고분자는 분자 사슬이 불규칙하게 배열된 비결정성 고분자 혹은 무정형 고분자와, 분자 간 상호작용이나 분자 내 상호작용에 의해 분자가 규칙적으로 배열되어 결정을 이룬 결정성 고분자로 분류할 수 있다. 고분자 내부에는 결정을 이루지 못하는 부분이 섞여 있게 되는데 결정 영역은 고분자의 역학적 강도를 높이는 역할을 하고 비결정 영역은 고분자를 더욱 유연하게 해 준다. 따라서 결정 영역을 조절하여 고분자의 역학 강도를 다양하게 조절할 수 있다. 고분자는 열적 거동이 무정형, 결정형, 액정에 따라 다르다. 무정형을 가열하면 유리 전이점을 지나 고무상태가 되고 차츰 액체가 된다. 결정형은 이와 달리 특정 용융점이 존재한다. 액정 고분자는 유리 전이점과 용융점 사이에 가용융점이 존재한다. 고무는 무정형 고분자를 쓰는데 가교 결합을 통해 고분자 사슬의 운동을 억제해 탄성이 생기게 할 수 있다. 또한 고분자는 분자 간 인력이 높으므로 물에 잘 녹지 않으며 물을 흡수하여 부피가 팽창하기 쉽다. 때로 투명한 고분자도 존재하는데 유리 전이 온도가 높고 고분자 사슬이 무질서하게 존재하여 빛을 잘 통과시키기 때문이다.
해설 및 핵심용어 정리
많은 고분자는 간단한 화학 구조를 가진 구조 단위가 수많은 공유 결합으로 연결된 사슬 형태의 분자이다. 이 공유 결합은 회전하여 다양한 입체 형태(conformation)를 취할 수 있으므로 고분자는 가능한 분자 형태가 매우 다양하다. 따라서 고분자는 응집 상태가 무질서할 수도 있고 분자 간이나 분자 내의 상호작용에 의해 질서정연한 응집 상태를 취할 수 있게 된다.
따라서 고분자는 분자 사슬이 불규칙하게 배열된 비결정성 고분자 혹은 무정형 고분자와, 분자 간 상호작용이나 분자 내 상호작용에 의해 분자가 규칙적으로 배열되어 결정을 이룬 결정성 고분자로 분류할 수 있다. 고분자는 보통 모든 고분자 사슬을 전부 규칙적으로 배열하기 어려우므로 결정을 이루지 못하는 부분이 섞여 있게 된다. 결정 영역은 고분자의 역학적 강도를 높이는 역할을 하고 비결정 영역은 고분자를 더욱 유연하게 해 준다. 만약 결정 영역이 조금이라도 있으면 비결정성 고분자가 아닌 결정성 고분자로 분류된다. 주로 고무는 유연한 비결정성 고분자가 쓰이고 섬유에는 셀룰로오스와 같은 결정 영역이 비교적 많은 결정성 고분자가 쓰이며 플라스틱에는 용도에 따라 비결정성 고분자와 결정성 고분자 모두 쓰인다. 특히 페놀 수지와 같이 화학 결합이 확장되어 분자 사슬에 친화력이 있는 용매를 가해도 용해되지 않고 가열하더라도 분자 사슬이 잘 떨어지지 않으므로 열경화성 수지나 흡수성 고분자로 많이 쓰인다.
고분자의 역학 강도는 저분자와 달리 다양하게 조절 가능하다. 결정성 고분자의 고체는 결정 영역과 비결정 영역이 혼재한다. 이 중 결정 영역에 따라 고분자의 경도와 강도가 달라진다. 따라서 결정 영역의 비율(결정화도)를 조절함에 따라 같은 고분자로부터 여러 가지 물성을 갖는 제품을 얻을 수 있다. 예를 들어 같은 폴리에틸렌이라 하더라도 분자량이 100만을 넘어서고 결정화도가 높은 고밀도 폴리에틸렌을 제조할 수 있다. 이런 폴리에틸렌은 역학 강도가 높아서 내충격 강도나 내마모성이 현저히 높고 기름 없이도 눌러 붙지 않는 자기윤활성도 우수하여 가혹한 조건 하에서도 사용 가능하다. 또한 고분자 사슬을 섬유 방향으로 배향시킨 실은 결정화도가 높아서 강도 또한 높다. 예를 들어 1mm2당 하중 약 500kg도 견디는 등 철강에 맞먹는 실도 만들어지고 있다. 폴리에틸렌뿐만 아니라 일반적인 고분자도 질서 있게 배열된 결정 영역과 흐트러진 비결정 영역이 혼재된 구조이다.
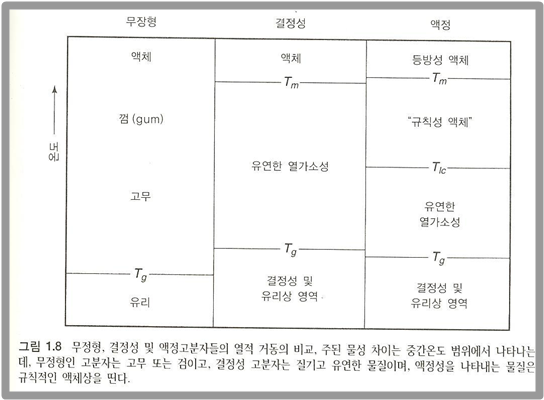
고분자의 열적 거동은 저분자와 크게 다르다. 저분자는 일반적으로 물질의 세 가지 상태인 고체, 액체, 기체 상태가 모두 존재한다. 그렇지만 고분자는 이와 다르다. 우선 동결 상태로 모든 분자가 움직이지 않는 상태일 경우에도 저분자와 같이 모든 분자가 결정으로 되어 있지 않고 비결정 영역이 존재하므로 전체적으로는 유리와 비슷한 상태가 된다. 이 상태에서 고분자의 온도를 높이면 어느 온도에서 먼저 비결정 영역에 있는 분자 사슬부터 움직이게 된다. 이러한 부분 운동을 ‘마이크로 브라운 운동’이라고 하고 비결정 영역의 분자 사슬이 마이크로 브라운 운동을 시작하는 온도를 유리 전이점(Tg)라고 한다. 유리전이점은 저분자량 화합물의 특성인 녹는점과는 다르다. 여기서 온도를 더 올리면 분자 사슬의 운동은 활발해지지만 분자 사슬이 얽혀 있으므로 여전히 고체로 보인다. 이러한 상태를 고무 상태라 한다. 온도가 더욱 올라가면 점차 액체가 되지만 특정 용융점(Tm)은 존재하지 않는다. 만약 결정 영역이 존재한다면 용융점이 존재하며 온도가 결정 영역의 용융점에 도달할 경우 유동성 있는 액체가 된다. 여기서 용융점이란 결정 영역의 분자 사슬이 중심 이동을 동반해 움직이기 시작하는 온도를 말하며 분자 사슬을 구성하는 구조 단위의 화학 구조에 따른 고유한 값이다. 어떤 고분자는 유리전이점과 등방성 액체 형성 온도 사이에 추가 상전이가 있을 수도 있는데 이러한 고분자를 액정고분자(liquid crystal polymer)라고 한다. 액정고분자는 열을 가하면 유리상과 미세결정상을 지나 가용융점(Tlc)dl존재하는데 이 온도부터 용융점까지는 액체와 비슷하다. 그렇지만 액체와 달리 곁사슬들이 이 상에서 느슨하게 쌓여 있으나 골격 부분은 배열을 유지하고 있다. 이러다가 용융점을 지나면 구조를 완전히 잃고 이방성 액체가 된다.
폴리에틸렌은 결정화도가 높으므로 비결정 영역의 유리 전이 온도를 아는 것은 곤란하며 어떻게 측정하느냐에 따라 -120도부터 0도 부근까지 달라질 수 있다. 한편 결정 영역의 융점은 110-140도이므로 0도부터 100도까지는 결정의 비율에 따른 역학 강도가 있는 고체가 된다. 폴리에틸렌이 플라스틱 바가지 등의 플라스틱 제품이나 필름으로 이용할 수 있는 것은 이런 특성 때문에 성형 가공을 할 수 있기 때문이다. 한편 비결정성 고분자는 유리 전이점을 넘어서면 고무 상태가 되고 따로 융점은 존재하지 않는다. 만일 더 온도를 높인다면 유동성 있는 고분자 액체로 변한다. 이를 액정 고분자와 비교하여 나타내면 다음과 같다.
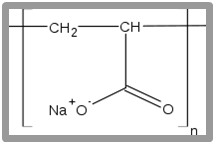
고무로 이용되는 고분자는 비결정성 고분자이다. 이 고분자의 유리 전이 온도는 일반적으로 -130도에서 -20도 사이이므로 실온에서 잘 모양을 바꿀 수 있다. 외력을 가하면 다시 원래 모양으로 돌아가지 않으나 구성 분자 사이에 가교 결합을 만들면 삼차원 그물 구조가 생겨 분자 전체가 결합된다. 각 고분자 사슬은 실온에서 마이크로 브라운 운동을 하고 있으므로 작은 힘만 가해도 쉽게 변형되나 힘을 가하지 않게 되면 분자 사슬이 자연스러운 원래 분자 형태가 되려고 하므로 탄성이 생긴다. 따라서 고무의 탄성은 유리 전이 온도보다 높은 고분자 사슬의 운동을 가교 결합으로 억제해 생긴 고분자의 특성이다. 또한 이렇게 가교 결합이 있는 고분자는 분자 사슬에 친화성이 높은 용매에 녹더라도 용해되지 않고 용매를 흡수하여 팽윤된다. 예를 들어 물에 녹는 소듐 폴리아크릴레이트(sodium polyacrylate)에 가교 결합을 가하면 물에 녹지 않고 원래 부피의 500배까지 물을 흡수할 수 있다. 이런 고분자를 고흡수성 고분자라고 하며 종이 기저귀, 생리용품 등에 쓰인다.
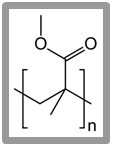
투명한 고분자도 존재한다. 폴리메틸메타크릴레이트(polymethyl metacrylate, PMMA)의 유리 전이 온도는 105도이므로 실온에서는 고분자 사슬이 동결되어 있다. 이 고분자의 고분자 사슬은 무질서하게 존재하므로 빛을 잘 통과시켜 매우 투명할 뿐만 아니라 유리보다 내충격성이 뛰어나고 가벼우며 성형 가공도 쉬워 비행기의 창문 재료, 수조, 안경용 렌즈 등에 쓰인다. 비결정성 고분자는 가공이 용이하므로 가는 실 형태로 뽑아 광섬유로 쉽게 사용 가능하므로 내시경이나 LAN선 등에 쓰인다.
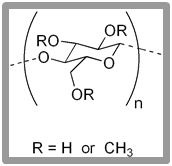
고분자는 매우 크므로 잘 용해되지는 않는다. 우선 셀룰로스를 그 구조 단위에 해당하는 글루코스와 비교해 보자. 글루코스 분자 간에는 수소 결합이 형성되므로 글루코스는 비교적 질서 있게 배열되어 결정 구조가 될 수 있다. 그러나 수소 결합은 강하지 않으므로 물 분자와 강하게 상호 작용하여 결정이 깨져 물에 용해된다. 그런 셀룰로스는 수소 결합을 해도 물에 녹지 않는다. 이 이유는 셀룰로스는 고분자 사슬 간에 수소 결합을 하여 분자 간 인력이 높기 때문이다. 그래서 셀룰로스가 물과 친화력이 높은 하이드록시기가 있는데도 물에 녹지 않는다. 그런데 셀룰로오스의 하이드록시기가 메톡시기로 바뀐 메틸 셀룰로스(methyl cellulose)는 물에 녹는다. 물과 메톡시기가 서로 상호작용을 하지 못하는데도 물에 녹는 이유는 하이드록시기가 만드는 결정 영역을 메톡시기가 없애기 때문이다.
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
이해가 안 되거나 궁금한 점이 있다면 커뮤니티에 질문해 보세요!
게시글 작성하기